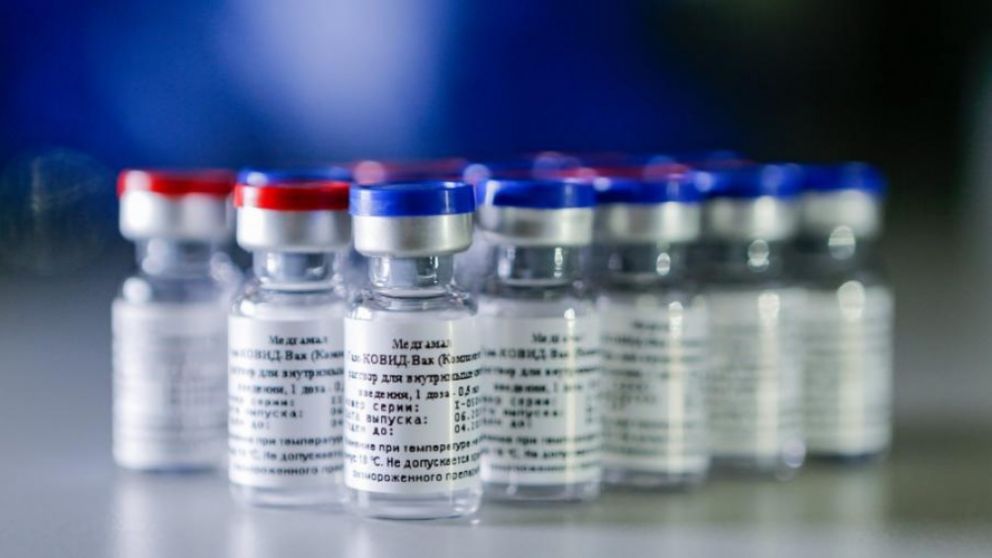
La vacuna rusa es segura, concluyeron los ensayos clínicos
Los investigadores de ese país publicaron sus resultados preliminares en la revista médica británica The Lancet. Ahora comenzarán con las pruebas a gran escala en fase III
La vacuna contra el coronavirus Sputnik V, desarrollada por Rusia, generó anticuerpos contra el virus y no provocó incidentes adversos, según los ensayos clínicos de los investigadores de ese país que publicaron el viernes sus resultados preliminares en la revista médica británica The Lancet. Ahora podrá avanzar hacia las pruebas a gran escala en fase III.
El grupo de expertos encontró que dos formulaciones -una congelada y otra liofilizada- de una vacuna que consta de dos partes son "seguras", pues no identificaron reacciones adversas de gravedad en más de 42 días e indujeron respuestas de anticuerpos en todos los participantes en un plazo de 21 días.
La formulación congelada está diseñada para su uso a gran escala, mientras que la liofilizada se desarrolla teniendo en mente aquellas regiones de difícil acceso, ya que pueden almacenarse a temperaturas de entre 2 y 8 grados centígrados, precisó la agencia EFE.
Los resultados secundarios de los ensayos (no tan relevantes como los primarios) también llevaron a pensar, según el informe, que las vacunas producen la respuesta de la denominada célula T en un plazo de 28 días, que detecta y mata patógenos invasores o células infectadas.
Los ensayos se llevaron a cabo en dos hospitales rusos con 76 adultos de entre 18 y 60 años, que se aislaron tan pronto se registraron para participar en las pruebas clínicas y permanecieron en los centros médicos durante los primeros 28 días.
Entre algunos de los hallazgos, vieron que ambas formulaciones resultaron seguras y se toleraron bien y entre los eventos adversos más comunes figuraron dolor en el lugar de la inyección (en un 58% de participantes), hipertermia (en un 50%), dolor de cabeza (un 42%), astenia (un 28%), y dolor muscular y de articulaciones (24%).
Sobre las "limitaciones" del estudio, los investigadores mencionaron el corto periodo de seguimiento (42 días); que se trate de una investigación "pequeña"; que algunas partes de la primera fase de los ensayos incluya solo a voluntarios varones y que no hubiese placebo.
En cuanto a los próximos pasos de la investigación, el profesor Alexander Gintsburg, del Centro Nacional de Investigación para Epidemiología y Microbiología (Rusia), dijo que la fase III del ensayo clínico de la vacuna incluirá 40.000 voluntarios de diferentes grupos de edad y de riesgo. Se espera que esta fase esté concluida hacia los meses de octubre o noviembre.
Además, se confirmó que será testeada en unas 10.000 personas en Brasil a finales del mes próximo.
El epidemiólogo Naor Bar-Zeev, del Centro internacional de Acceso a Vacunas (EE.UU.), ajeno a la investigación, alertó, por su parte, de que todos los candidatos a vacuna deben mostrar "que son seguros y probar una eficacia clínica duradera (que incluya a grupos de mayor riesgo) en ensayos grandes aleatorios antes de que puedan ser utilizados".
El origen de la polémicaEl 11 de agosto pasado, el presidente de Rusia, Vladimir Putin, anunció oficialmente que su país tenía una vacuna contra el coronavirus, la primera aprobada en el mundo.
Sin embargo, hasta ahora Rusia no había aportado detalles de las pruebas clínicas, y presentó su vacuna antes de realizar los ensayos en fase III, algo que generó inquietud y cierto escepticismo en el mundo científico.
En ese sentido, la Organización Mundial de la Salud (OMS) expresó entonces su cautela frente al anuncio de Putin, y recalcó que "acelerar los progresos no debe significar poner en compromiso la seguridad".
Ahora, sin embargo, el informe publicado en The Lancet vino a arrojar luz sobre el asunto, aunque todavía faltan las pruebas a una escala mayor.